病痛罕见,爱不罕见,关注罕见病,MORE Health爱医传递在行动!
他们是一群遗落在凡间的天使,他们生而罕见,却不愿放弃,一步一步向前追寻生的希望。

“瓷娃娃”(脆骨病)、“月亮孩子”(白化症)、“不食人间烟火的孩子”(苯丙酮尿症)……这些听上去有点浪漫的名字,背后却是可怕的疾病。它们同属于流行率很低、80%由基因缺陷所导致的疾病,全世界范围内的近7000种病症奇异、发病率低但死亡率高的疾病统称为罕见病。
2008年2月29日,欧洲罕见病组织(EURODIS)发起了第一届国际罕见病日。选择此时间点是由于这是每四年才出现一次的日子,寓意“罕见”。其后在各国的一致拥护下,将每年二月的最后一天定为国际罕见病日。

根据世界卫生组织报道,约有80%的罕见病由于遗传缺陷引起,约有50%的罕见病在出生时或者儿童期即可发病。罕见病常进展迅速,死亡率很高,仅有约1%的罕见病有有效治疗药物。
由于发病率极低、不会造成大面积的流行等因素,使得罕见病的受重视程度比较低下,至今尚无被广泛认可的罕见病定义。在尚无确切定义的情况下,罕见病病理研究和药物研发都难以得到社会的广泛认可和相关政策的倾斜。
近年来随着全球对罕见病的日益重视和关注,罕见病的发展取得了一系列突破。
目前,全球已有30多个国家先后从立法方面对罕见病用药研发及治疗方面给予了保障和支持。例如,日本对罕见病用药研发公司给予10%的税务减免;韩国对罕见病用药报销2/3的费用;欧盟则给予研发公司长达10年的市场独占期;美国通过《罕见病用药法》,这些优惠政策及法规也直接刺激了各国罕见病药物研发市场。

但在中国,目前市场上销售的罕见病用药几乎全部依赖进口,同时关于罕见病药物研发的专项法律也是一片空白,罕见病患者的服务机构也极少。对罕见病官方定义的缺失,被认为是目前罕见病相关政策制定的困难和瓶颈。
值得庆幸的是,现在我国正在努力填补罕见病领域的空白。2016年1月4日,中华人民共和国国家卫生和计划生育委员会官网发布:为加强罕见病管理,促进罕见病规范化诊疗,保障罕见病用药基本需求,维护罕见病患者的健康权益,国家卫生计生委组建了国家卫生计生委罕见病诊疗与保障专家委员会。
另外,2016年2月26日,CFDA发布的《关于解决药品注册申请积压实行优先审评审批的意见》文件明确指出,治疗罕见病的药品可享受注册申请优先审评审批。这对中国孤儿药的研发与审批而言,无疑是良好的开端。
这些法规政策也促进了我国罕见病领域用药市场的良好发展,引领更多医药企业进军该市场。相信在国家政策扶持及社会关注度越来越高的情境下,我国罕见病治疗在未来一定会有突破性的进展。

罕见病药物:
在过去的2017年,美国FDA批准了数种罕见病药物:
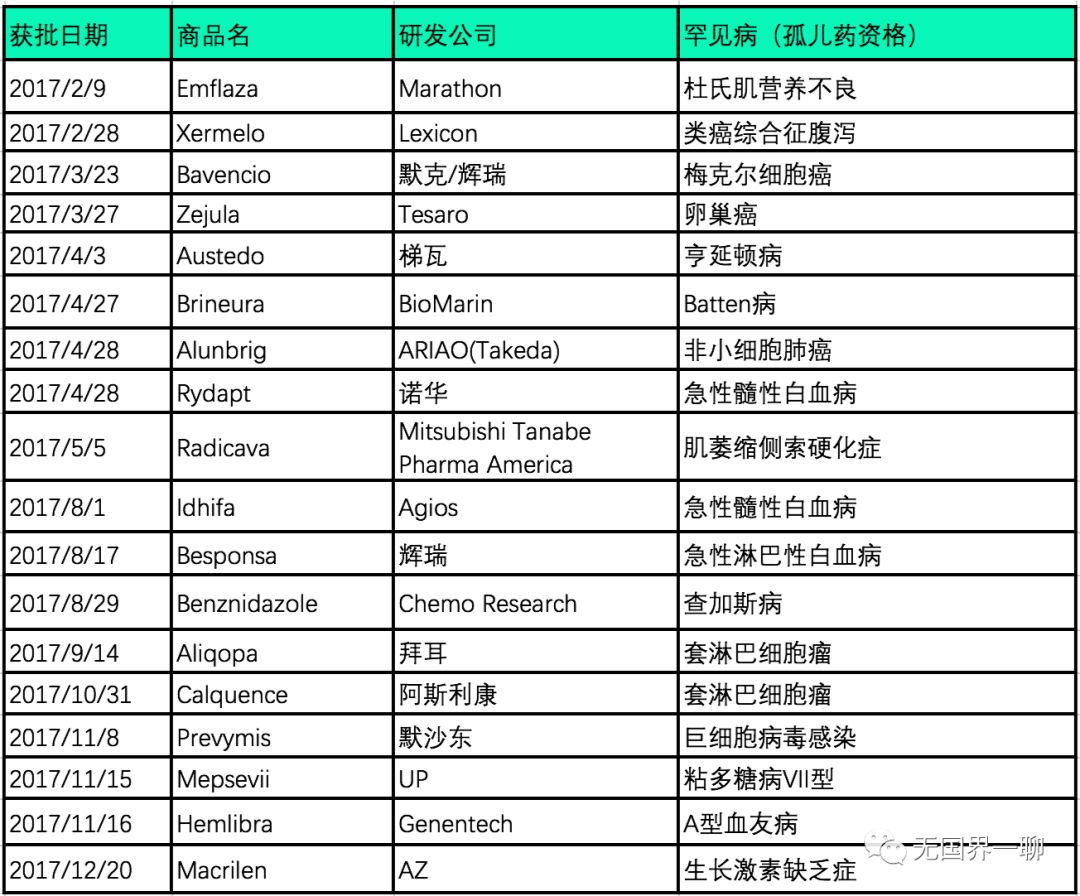
MORE Health爱医传递作为一家专注于危重疑难疾病的美国顶级医疗服务机构,近年来也一直关注并致力于罕见病的发展,我们希望将美国最新的罕见病治疗方法及可用药品带给广大中国患者,使罕见病患者可以多一丝希望,不再忍受病痛的折磨,关注罕见病,我们在行动!
 全国服务热线 400-076-3808
全国服务热线 400-076-3808



 (1).png?imageView2/1/w/200/h/150/format/jpg/interlace/1/q/65|imageslim)





 在线客服
在线客服 在线预约
在线预约 常见问题
常见问题

